首页能源头条推荐资讯详情
FEC与VC在锂离子电池石墨负极界面行为研究
发布者:
来源:
DOI:10.19799/j.cnki.2095-4239.2025.0217
本文亮点:1.利用三电极扣电准确监测到了石墨电极表面的动力学信息 2.发现了FEC与VC在石墨界面上的不同作用机制 3.利用EIS-DRT准确解耦出了锂离子电池高频区发生的四个电极过程,并确定其弛豫时间。
摘 要 在锂离子电池中,电解液添加剂如氟代碳酸乙烯酯(FEC)和碳酸亚乙烯酯(VC)被广泛用于改善电极/电解液界面的稳定性,但是其对石墨电极表面的作用机制仍不清晰。本工作系统研究了FEC和VC在锂离子电池石墨电极上的界面行为。通过循环伏安法、电化学阻抗谱、扫描电子显微镜、透射电子显微镜和X射线光电子能谱等多种表征手段,揭示了FEC和VC在石墨电极表面的差异化作用机制。电化学阻抗结果显示Li|Gr电池中FEC形成固体电解质界面(SEI)前后的总阻抗小于VC,Li|Ref|Gr电池中FEC形成SEI前后的总阻抗大于VC。通过电化学阻抗谱-弛豫时间分布(EIS-DRT)方法,进一步对界面阻抗进行剖析,确定了FEC和VC在Li|Gr电池中的SEI阻抗、SEI-Gr界面电荷交换阻抗、SEI-电解液界面电荷交换阻抗的特征弛豫时间范围,FEC与VC各部分的弛豫时间基本一致,SEI阻抗、SEI-Gr界面电荷交换阻抗、SEI-电解液界面电荷交换阻抗弛豫时间分别为5E-5 s、3E-4 s、5E-3 s。研究结果表明,VC在0.77 V还原形成富含有机物的SEI,可显著降低石墨界面的阻抗,但其与锂金属的相容性较差,导致电池总阻抗增加。而FEC在1 V电压下还原,在石墨表面形成富含LiF的SEI,虽然使得石墨界面阻抗增加,但是显著优化了锂金属对电极的稳定性。FEC对石墨界面的劣化影响小于对锂金属的稳定优势,使得电池总阻抗最小。本研究为锂离子电池电解液的优化设计提供了重要的实验技术和理论指导。
关键词 锂离子电池;电极/电解液界面;氟代碳酸乙烯酯;碳酸亚乙烯酯
锂离子电池作为高效、可靠的能源存储技术,在电动汽车、便携式电子设备以及可再生能源存储系统中占据了重要地位。其高能量密度、长循环寿命和较低的自放电率使其成为现代能源存储领域的核心选择。在锂离子电池的研究中,固体电解质界面(SEI)作为锂离子电池的重要组成部分,对电池的电化学性能、循环稳定性和安全性具有深远影响。特别是在电池的初次充放电过程中,电解液的界面分解行为直接决定了SEI膜的形成及其特性,进而影响电池的长期性能。电解液添加剂是改善界面问题的有效策略之一。氟代碳酸乙烯酯(FEC)和碳酸亚乙烯酯(VC)因其对SEI膜的优化作用而备受关注。FEC作为一种高效的电解液添加剂,已被证明能够显著改善锂离子电池的循环性能和倍率性能。研究表明,FEC在高电位下优先还原,生成富含LiF的SEI膜,这种膜具有较高的机械稳定性和离子导电性,能够有效抑制电解液的进一步分解和电极材料的副反应。此外,FEC的引入还能够减少石墨电极表面的锂沉积,从而提高电池的安全性。VC是另一种被广泛研究的电解液添加剂,其通过在正极和负极表面形成稳定的SEI来改善电池性能。VC的还原电位较高,能够在电池充放电初期形成均匀且致密的SEI膜,从而有效抑制电解液的持续分解和电极材料的体积膨胀。研究还表明,VC的少量加入能够减少电池在高倍率充放电过程中的极化现象,从而提高电池的倍率性能。然而,FEC和VC在不同电极界面上的差异化行为及其对全电池性能的影响机制尚未得到系统研究。传统的研究方法往往局限于全电池测试,全电池测试耦合了正极和负极的信息,难以区分添加剂在正负极界面上的具体作用。在两电极电池中植入参比电极,构建三电极体系便可以很好地解决上述问题,单独研究每个电极的界面特性及其对整个电池的影响。
本工作系统研究了FEC和VC在石墨电极表面的界面行为。通过循环伏安法(CV)、电化学阻抗谱(EIS)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)和X射线光电子能谱(XPS)等手段,揭示了FEC和VC在SEI膜形成过程中在石墨电极上的作用机制。引入电化学阻抗谱-弛豫时间分布(EIS-DRT)方法将EIS数据分解为多个具有明确物理意义的弛豫过程。结果表明VC与FEC在石墨电极表面分别在0.77 V和1 V电压下优先还原,对电池动力学产生不同的影响,添加剂FEC在石墨电极表面的界面阻抗大于VC,但是对于整个电池的总阻抗小于VC,并且将Li|Gr电池高频区的阻抗来源解耦为四个部分:接触阻抗(弛豫时间约1E-5 s)、SEI膜阻抗(弛豫时间约5E-5 s)、SEI-Gr界面阻抗(弛豫时间约3E-4 s)和SEI-电解液界面阻抗(弛豫时间约5E-3 s),其中SEI-电解液界面阻抗为电荷转移的决速步骤。VC在石墨表面形成以胶状聚合物为主、少量Li2CO3为辅的SEI膜。这种SEI膜在短期内表现出较低的界面阻抗,有利于石墨电极的快速充放电性能。相比之下,FEC在石墨电极表面形成的SEI膜富含LiF,具有更加致密的形貌结构,导致石墨电极界面阻抗略高于VC。但是FEC对锂金属界面的优化效果更为显著,能够有效降低整体电池的阻抗。
1 实验部分
1.1电解液配置
电解液的配置过程中需注意操作环境(如无水无氧环境)和试剂纯度,以确保电解液的稳定性和电池性能,所以电解液均在手套箱内配置而成。电解液DE73按体积比3∶7量取碳酸乙烯酯(EC)和碳酸二甲酯(DMC),将两种溶剂混合均匀,确保充分溶解,EC在使用前利用加热台加热熔化。再称取1.0 mol/L的六氟磷酸锂(LiPF6),将LiPF6缓慢加入混合溶剂中,搅拌至完全溶解。对于液体添加剂碳酸亚乙烯酯(VC)、氟代碳酸乙烯酯(FEC)按总电解液体积的1.0%加入配置好的基础电解液DE73中,分别命名为DE73+1%VC和DE73+1%FEC。按照上述配置方法再配置0.1 mol/L LiPF6 VC和0.1 mol/L LiPF6 FEC电解液,分别命名为VC,FEC。所有电解液都需要储存在干燥、密封的容器中,避免接触水分和空气。
1.2电极片的制备
用于阳极的石墨浆料在离心混合器(Kakuhunter,SK-300 SII)中通过多步混合工艺制备。采用刮涂法制备了石墨(Gr,江西紫辰科技有限公司)阳极极片。石墨阳极浆料质量配比Gr∶Super P∶PVDF为90∶4∶6,石墨作为活性物质;Super P作为导电剂;聚偏二氟乙烯(PVDF)作为黏合剂,通常溶解在1-甲基-2-吡咯烷酮(NMP)中配成质量分数为5%的溶液保存使用,最终配好的浆料固体含量为30%。将石墨阳极用刀高为100 μm的刮刀涂覆在铜集流体(铜集流体厚度为11 μm)上,阳极的活性材料负载为2.55 mg/cm2(0.94 mAh/cm2)。阳极电极被冲压成直径为10 mm的电极圆片,用于组装纽扣电池。电极片在100 ℃下真空干燥12小时后再使用。
1.3电池组装
电池组装以Li|Gr电池为例,Li|Gr电池采用对称电池结构组装,工作电极为石墨,对电极为锂金属。Li|Gr两电极扣式电池如图1(a)所示,Li|Ref|Gr三电极扣式电池组装如图1(b)所示,在两电极的基础上引入锂镀覆的铜参比电极。Li|Cu电池将石墨换为铜光箔即可。所有组装过程均在充满氩气手套箱中进行,以避免水分干扰。
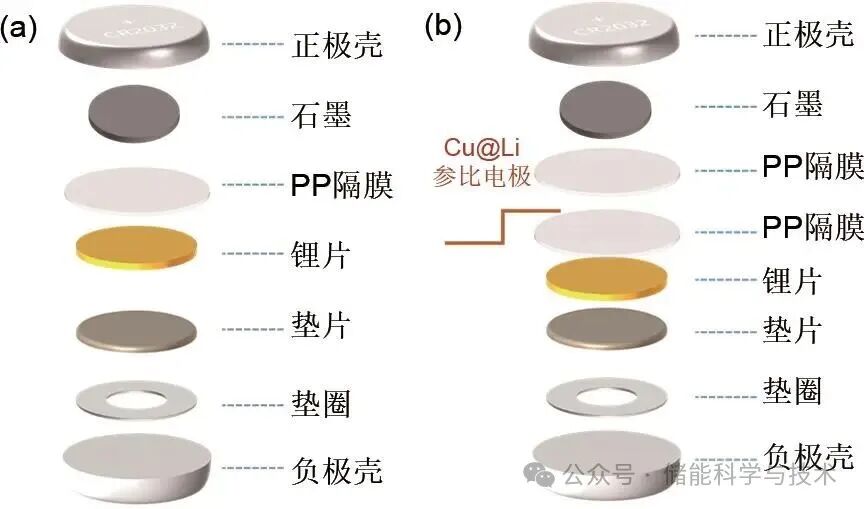
图1 (a) 两电极纽扣电池组装图;(b) 三电极纽扣电池组装图
2 结果与讨论
2.1电解液本征特性
电解液的电导率是评估其离子传输性能的重要参数,直接影响锂离子电池的倍率性能和循环稳定性。为探究FEC和VC添加剂对电解液电导率的影响,本研究对电解液的电导率进行了精确测量。测试结果如表1所示。加入添加剂FEC和VC后电解液的电导率均增加了0.15 mS/cm,且两种加了电解液添加剂的电解液电导率相同,说明它们在离子传输性能上表现相似。
表1 各电解液电导率

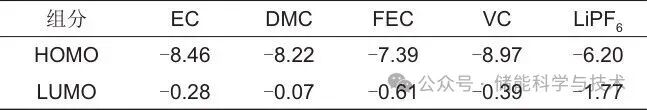
为了探究FEC和VC的还原顺序,本工作首先通过理论计算明确了不同电解液组分的最高占据分子轨道(HOMO)和最低未占据分子轨道(LUMO)的能级。如表2所示,FEC和VC的LUMO能级分别为-0.61 eV、-0.39 eV。LUMO能级越低,还原电位越高,由此可知在首次放电过程中各电解液组分的还原顺序,如图2(a)所示,由高电位到低电位依次是LiPF6、FEC、VC、EC、DMC。图2(b)是0.1 mol/L LiPF6分别溶解于FEC与VC单溶剂所制备电解液的LSV测试结果,依据前文得到的还原顺序,FEC中1.74 V的还原峰归属于LiPF6,FEC在1.12 V时发生还原;VC中,LiPF6还原电位为1.5 V,VC还原电位为0.85 V。LiPF6在FEC和VC中的还原电位不同说明溶剂环境会影响LiPF6的还原电位与反应程度。在基础电解液DE73中添加FEC和VC,由于化学环境的变化,还需要考虑溶剂的影响,所以FEC和VC的还原电位会发生略微偏移。图2(c)是电解液DE73、DE73+1%VC和DE73+1%FEC的CV测试结果,在DE73+1%VC和DE73+1%FEC中,FEC与VC的还原顺序保持与LSV中相同的结果,但是还原电位略有下降,FEC的还原电位为1 V,VC的还原电位为0.77 V,这可能是溶剂与溶剂之间的相互作用导致的。
表2 电解液各组分的HOMO, LUMO能级( eV )
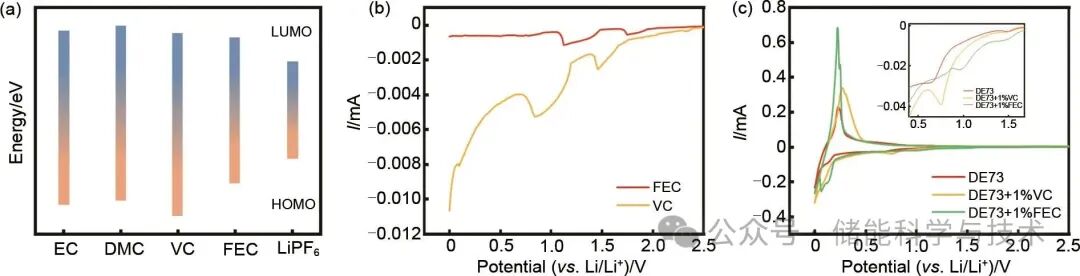
2.2VC与FEC对石墨界面的差异化影响
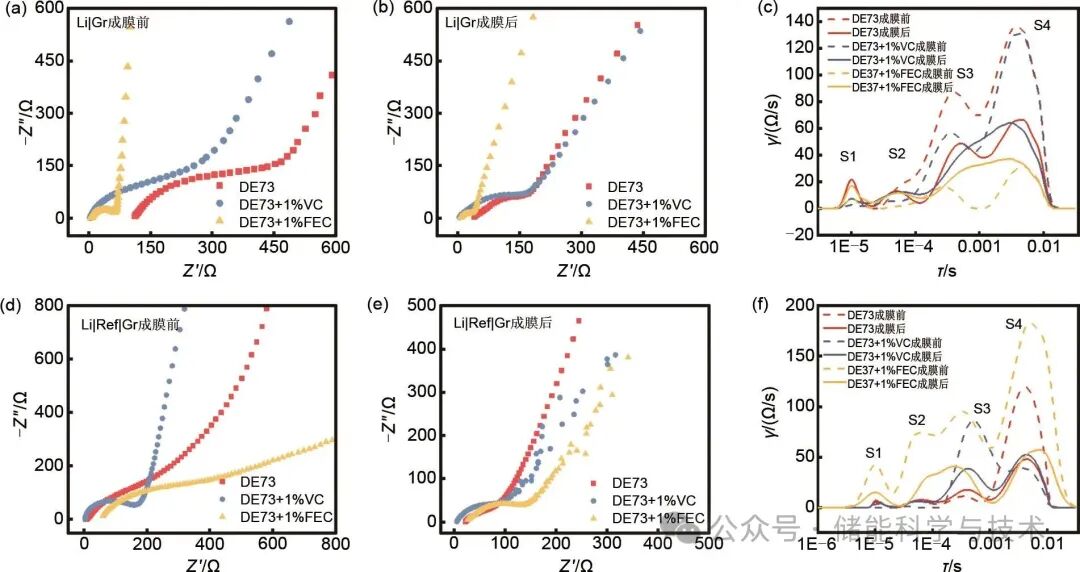
为了深入研究VC和FEC还原形成的SEI膜对石墨电极界面动力学的影响,本工作分别在Li-Gr的两电极池和三电极池中对DE73、DE73+1%VC、DE73+1%FEC成膜前后进行了EIS测试,并使用DRT对其阻抗数据进行解析。两电极和三电极的测试区别在于:两电极电池测量的是整个电池的总阻抗,包含了正极,负极和电解液三部分的贡献。而三电极测试,就本工作而言是在工作电极石墨端植入的参比电极,排除了锂金属对电极的影响,则此时三电极电池测试的电池仅包含石墨电极和电解液的贡献。这样就可以将VC和FEC对石墨和锂金属的影响分离开。由于两种电解液的离子电导率相同,可姑且认为电解液的体相电阻贡献是一致的,则本工作中三电极和两电极的阻抗仅相差一个锂对电极的阻抗RLi。
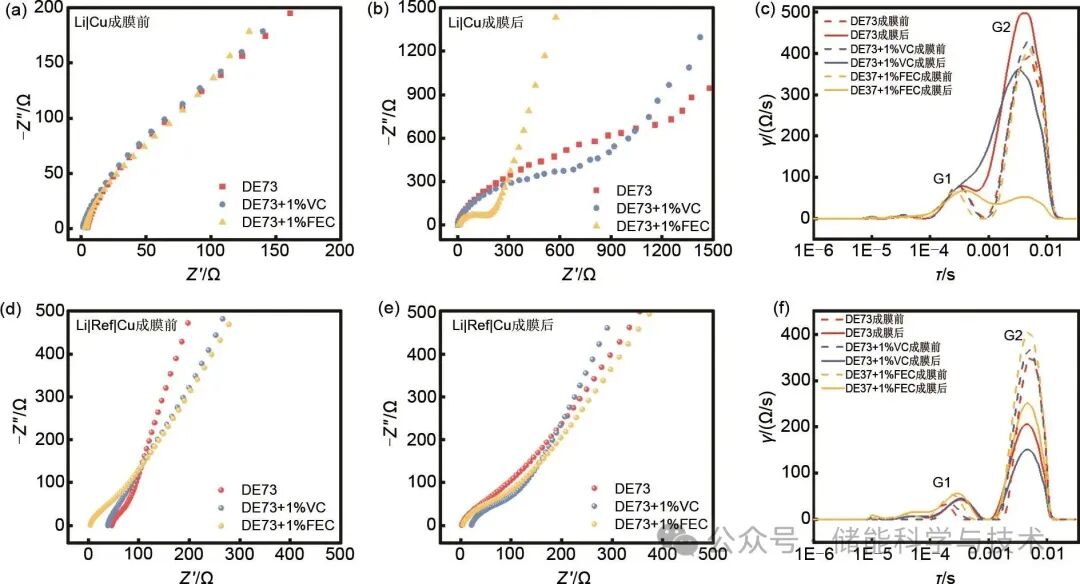
首先如图3(a)所示,在Li|Gr电池中,SEI形成前后,DE73+1%FEC的高频区欧姆环最小,其次是DE73+1%VC,未加添加剂的DE73阻抗最大,此时阻抗主要与电荷交换阻抗有关。SEI形成之后,如图3(b)所示,在两电极电池中,添加FEC和VC后,形成的欧姆环减小,表明高频区总阻抗均有所减小,但两者的减小幅度不同,表明添加剂在初始还原反应中起到了不同的作用。其中FEC表现出最低的高频阻抗,说明在两电极电池中FEC的整体表现优于VC。对高频区的阻抗数据进行DRT解析,如图3(c)所示,在Li-Gr电池中,出现了四个峰,每个峰都代表一个电极过程。依据文献报道的研究结果,S1、S2、S3、S4峰分别代表接触阻抗,SEI膜阻抗,电荷交换阻抗,超高频阻抗一般为接触阻抗,高频区为SEI膜阻抗,中高频区为电荷交换阻抗,接触阻抗一般指的是活性材料的体电阻及其与集流体导电炭网络之间存在的电阻。所以S1为接触阻抗、S2为SEI膜阻抗、S3、S4为电荷交换阻抗,弛豫时间分别为1E-5 s、5E-5 s、3E-4 s、5E-3 s。DRT分析显示DE73+1%FEC的S2、S3、S4都是最小的,DE73的S1,S2、S3、S4是最大的,而且S4为决速步骤。如图3(d)、(e)所示,在三电极电池的阻抗测试中,DE73+1%VC阻抗是最小的,DE73+1%FEC的阻抗反而是最大的。如图3(f)所示,DRT分析显示DE73+1%FEC的S1、S2、S3、S4都是最大的;DE73+1%VC的S1、S2是最小的;DE73的S3、S4是最小的,而且依然是S4为决速步骤。两电极和三电极EIS结果恰好相反的原因涉及到FEC和VC分别对石墨和锂金属的不同影响。当使用三电极测试时,DE73+1%VC的阻抗最小,说明单独测试石墨电极阻抗时,VC添加剂更有助于形成更优的SEI膜,降低了石墨界面上的阻抗。但在两电极中,总阻抗显示DE73+1%FEC阻抗更低,这意味着FEC对金属锂对电极的界面阻抗有着更积极的作用,从而才使整体阻抗更低。而VC虽然显著优化了石墨表面的SEI膜,但是却对锂金属界面有着劣化的影响或者未能有效抑制锂金属的界面问题,导致总阻抗反而更高。
为了排除石墨电极的影响,本研究组装了Li|Cu电池和Li|Ref|Cu电池来进行验证。结果如图4(a)~(d)所示,Li|Cu电池中DE73+1%FEC的阻抗最小,DE73的阻抗最大;Li|Ref|Cu电池中DE73+1%FEC的阻抗最大,DE73+1%VC的阻抗最小。DRT解析结果如图4(c)、(f)所示,Cu电极上不存在活性材料,所以Li|Cu电池和Li|Ref|Cu电池接触阻抗可以忽略不计,高频区只存在SEI膜阻抗和电荷交换阻抗,则图4中的峰G1和G2分别是SEI膜阻抗和电荷交换阻抗,弛豫时间分别为2E-4 s,5E-3 s。结合上文提到的Li|Gr电池和Li|Ref|Gr电池的DRT结果,可以对Li|Gr电池S3、S4峰进行准确地归属。Li|Cu电池与Li|Gr电池相差一个SEI与石墨之间的界面,所以S4与G2均为电荷交换过程且弛豫时间一致,应属于同一过程,即SEI-电解液界面电荷交换阻抗,则S3为SEI-Gr界面电荷交换阻抗。由图3和图4的测试结果可知VC和FEC对石墨电极界面有不同的优化效果。VC形成的SEI更有利于降低石墨电极的界面阻抗,但可能对锂金属对电极的界面有负面影响,如增加副反应或枝晶生长,导致总阻抗上升。而FEC虽然在石墨电极上的SEI效果稍逊,但能有效稳定锂金属界面,降低其界面阻抗,从而在两电极测试中总阻抗更低。
为了证实VC对锂金属对电极的不兼容以及FEC对锂金属对电极的稳定优化作用,本工作随后在Li-Li对称电池中进行了过电势测试。如图5所示,通过对比DE73、DE73+1%VC、DE73+1%FEC的电压时间曲线,可以发现DE73+1%FEC的过电势最低,为0.08 V,而DE73+1%VC的过电势为0.15 V,这恰恰证明了上述的结论。
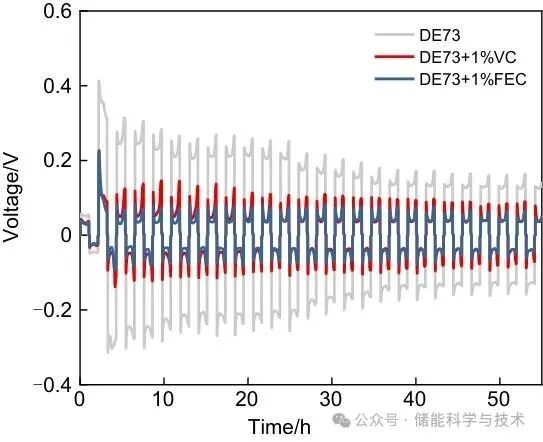
图5 Li-Li对称电池镀锂/剥离过程的电压-时间曲线
2.3SEI膜的形貌结构和组分差异
为了进一步探究FEC和VC在石墨电极上存在不同界面行为的原因,本工作首先对在三种电解液中循环后的电极表面进行分析,通过SEM、TEM确认SEI的形貌结构差异,对成膜后的石墨极片进行了SEM和TEM的表征。SEM图像分别展示了在DE73,DE73+1%VC,DE73+1%FEC电解液中循环后电极表面的微观结构特征。如图6(a)~(c)所示,未添加任何添加剂的基础样品DE73中形成的石墨表面呈现出光滑的表面形貌。当添加1%的VC时,可以观察到石墨表面形貌发生了显著变化,其微观结构显示出典型的颗粒分布且表面纹理颗粒间的结合更为紧密,表面粗糙度有所增加,这可能表明VC的添加影响了石墨表面的结晶行为或表面能。添加1%的FEC后,石墨表面显示出更为复杂的表面结构,颗粒尺寸和形状发生了明显变化,颗粒分布更加均匀。总之SEM结果显示,FEC的添加使得SEI膜更加致密且均匀,VC则形成了较为松散的SEI膜。TEM结果进一步证实了这一点,如图6(d)~(f)所示,没有加添加剂的DE73的SEI膜则呈现分布不均匀的状态;VC形成的SEI呈现果胶状,较为疏松的SEI膜形态,厚度较薄大概为5 nm,而FEC形成的SEI膜结构更加均匀致密且稳定,厚度大概在7 nm,具有较好的机械强度,从而能有效阻止电解液与石墨负极的直接接触,但是会带来较大的界面阻抗。

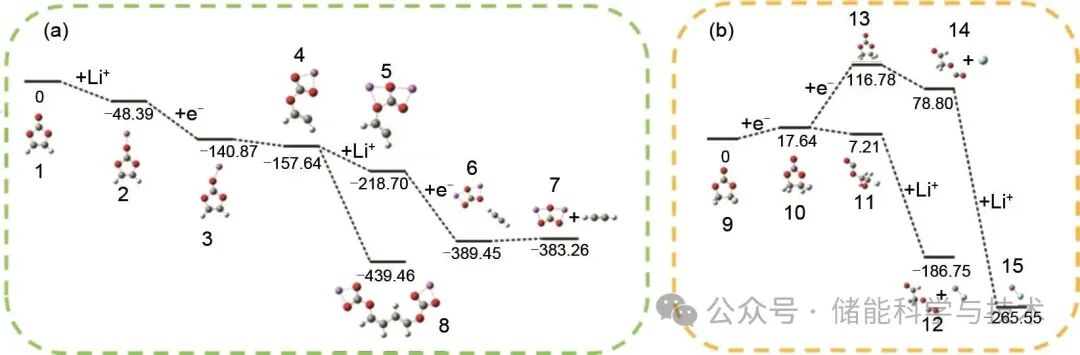
为了探究VC与FEC形成的SEI成分的差异,本研究首先通过理论计算对FEC和VC的还原路径进行理论模拟。由于溶剂的还原分解伴随着Li+的参与,因此本工作借助密度泛函理论(DFT)研究了VC/Li+和FEC/Li+的还原机理,得到了VC和FEC与Li+结合后的还原反应自由能台阶图。图中的数据是在b3lyp/6-311+g(d, p)级别下进行几何优化和能量计算,并使用色散校正DFT-D3(BJ)以准确描述弱相互作用下获得的。如图7(a)所示,VC反应物通过极性O原子与Li+结合形成活化中间体VC-Li+反应物2,反应自由能为-48.39 kcal/mol。反应物2获得一个电子形成反应物3,VC-Li+化合物,反应自由能为-140.87 kcal/mol。VC-Li+容易得到反应物4,CHCHCO3Li,反应自由能降低了16.77 kcal/mol,到此步骤说明VC容易发生单电子反应生成CHCHCO3Li。之后反应物4继续与锂离子结合成活性中间体5,CHCHCO3Li2。反应物5得到一个电子,生成反应物6,反应自由能降低为-389.45 kcal/mol。反应物6分解生成产物7,Li2CO3和C2H2,反应自由能为-383.26 kcal/mol。此外,两个反应物4自发聚合形成自由能更低(-439.46 kcal/mol)的产物8,(CHCHCO3Li)2,这可能是VC还原形成的SEI膜中的一个关键组分。图7(b)是FEC的分解路径图,FEC分子上含有一个高电负性的F原子,吸引电子能力强。反应物9,也就是FEC得电子,生成反应物10,CH2CHFCO3,反应自由能为17.64 kcal/mol。10之后有两个反应路径,一个是继续得电子使得C=O键活化形成反应物13,13分解形成反应物14,F—,CO,CH2OCHO。F—与锂离子结合生成产物15,LiF,反应自由能为-265.55 kcal/mol。反应物10另一个反应路径是,F继续靠近五元环上的O,使得环上的C—O键断裂,形成活性中间体11,CO2CH2CHO和F—,中间体11与锂离子结合,最终生成产物12,CHOCH2O和LiF,反应自由能为-186.75 kcal/mol。整体反应路径来看,FEC还原分解更容易生成LiF。简言之,DE73+1%VC会生成含有更多有机聚合物(CHCHCO3Li)2 以及少量Li2CO3的SEI膜,而DE73+1%FEC会生成富含LiF以及少量CH2OCHO的SEI膜。
为进一步验证SEI膜的化学组成,本工作又采用XPS对成膜后的石墨电极进行了表征分析。SEI膜的O1s和F1s谱图分析结果如图8所示,在F1s谱图中,684.7 eV、686 eV、687 eV和688 eV处的特征峰分别对应于LiF、LixPOyFz、LixPFy和LiPF6。O1s谱图中,534.5 eV、533 eV和532 eV处的特征峰分别归属于LixPOyFz、C—O和C=O。
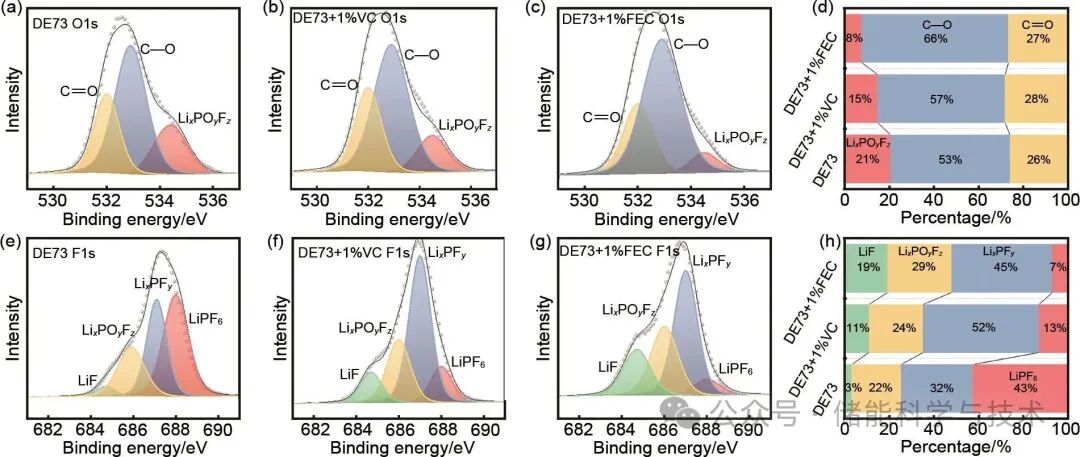
定量分析结果表明,在DE73+1%FEC体系中,SEI膜的F1s组分分布为:LiF(19%)、LixPOyFz(29%)、LixPFy(45%)和LiPF6(7%);DE73+1%VC体系中,相应组分的含量分别为11%、24%、52%和13%;而在DE73体系中,LiF含量最低(3%),其余组分分别为LixPOyFz(22%)、LixPFy(32%)和LiPF6(43%)。DE73+1%FEC体系中的LiF含量最多,这正好佐证了上文的计算预测结果:FEC还原形成更多LiF。O1s谱图分析显示,DE73+1%FEC形成的SEI膜中C—O键含量最高(66%),显著高于DE73+1%VC(57%)和DE73(53%)体系。对于DE73中的C—O大部分归因于EC的还原产物烷基碳酸锂,而FEC中的C—O键大部分来源于CHOCH2O和Li2CO3,而VC中的C—O键主要来源于(CHCHCO3Li)2。值得注意的是,SEI膜中LiF等无机组分的增加会显著提高膜的致密性和阻抗特性。DE73+1%FEC体系中较高的LiF含量(19%)与三电极测试中的阻抗结果及TEM观察到的致密SEI膜形貌相吻合。相比之下,DE73+1%VC体系中富含有机组分(CHCHCO3Li)2,这种组成特征导致SEI膜结构较为疏松且阻抗较小,这与三电极测试中观察到的低阻抗特性以及TEM显示的疏松结构特征相一致。
3 结 论
本研究通过多种表征手段(包括循环伏安法、电化学阻抗谱、扫描电子显微镜、透射电子显微镜和X射线光电子能谱)系统研究了FEC和VC对电解液稳定性及石墨电极界面行为的影响机制,为优化电解液配方和提升锂离子电池性能提供了重要的实验依据。研究结果表明,尽管VC与FEC在电解液中的溶解性和离子迁移能力相近,但它们在石墨电极界面上的行为表现出显著差异。通过电化学阻抗谱-弛豫时间分布(EIS-DRT)方法对阻抗数据进行解析,发现石墨电极上的阻抗来源可解耦为四个部分:接触阻抗(弛豫时间约1E-5 s)、SEI膜阻抗(弛豫时间约5E-5 s)、SEI-Gr界面阻抗(弛豫时间约3E-4 s)和SEI-电解液界面阻抗(弛豫时间约5E-3 s)。其中,SEI-电解液界面阻抗为电荷转移的决速步骤。VC在石墨表面优先还原,形成以胶状聚合物为主、少量Li2CO3为辅的SEI膜。这种SEI膜在短期内表现出较低的界面阻抗,有利于石墨电极的快速充放电性能。然而,VC与锂金属的相容性较差,容易引发锂金属表面的副反应,导致锂金属极化增加,进而影响电池的循环稳定性和安全性。相比之下,FEC在石墨电极表面形成的SEI膜富含LiF,具有更加致密的形貌结构,导致石墨电极界面阻抗略高于VC。但是FEC对锂金属界面的优化效果更为显著,能够有效降低整体电池的阻抗。本研究揭示了VC和FEC在不同电极界面上的差异化行为:VC通过牺牲锂金属界面的稳定性,换取了石墨SEI膜的短期低阻抗;而FEC则以略微增加石墨SEI膜阻抗为代价,显著提升了锂金属界面的稳定性。这一发现表明,在实际电池电解液设计中,需综合考虑电解液对正负极的兼容性。此外,本研究引入的EIS-DRT方法为SEI膜的形成机制提供了新的研究视角,为深入理解电解液添加剂的作用机制奠定了理论基础。
第一作者:赵岩(2000—),女,硕士研究生,研究方向为电化学储能器件技术开发
反馈举报
声明:以上信息仅代表发布者自身观点,并不代表本平台赞同其观点,也不代表本平台对其真实性负责。
评论 0
网友评论仅供其表达个人看法,并不表明平台立场。全部评论
加载失败
总发布:2083粉丝:5
相关推荐
- 加载失败
- 加载失败
- 加载失败
- 加载失败
九天能源公司
- 加载失败
能源行业新闻
- 加载失败
- 加载失败
- 加载失败
浙江数控能源
- 加载失败
旧能新能都是能
- 加载失败
浙江数控能源







